Nun erklären wir dir als angehenden Techniker die Energiebilanzen der Enthalpie beschrieben werden und welche Einflüsse zu berücksichtigen sind.
“Die Enthalpie ist ein Maß für den Energiegehalt eines thermodynamischen Systems. In der Regel wird diese mit dem Buchstaben H ausgedrückt und in der Einheit J (Joule) angegeben.”

Die Energiebilanzen der Enthalpien sind immer dann von Interesse wenn eine praktische Anwendung vorliegt.
Enthalpie – Reaktionsenthalpie und Umwandlungsenergie – Formel
In der nächsten Gleichung sind sowohl die Reaktionsenthalpie als auch die Umwandlungsenergie berücksichtigt:
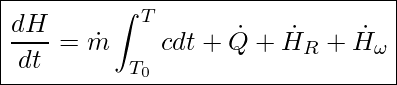
Kennzahlen:
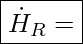 Reaktionsenthalpie
Reaktionsenthalpie
sowie
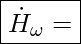 Umwandlungsenergie
Umwandlungsenergie
Enthalpie – Offene thermodynamische Systeme
Im nachfolgenden Bild siehst du ein Beispiel für ein offenes thermodynamisches System in Form einer Kaffeetasse mit Inhalt:

Im Falle von kontinuierlich offenen thermodynamischen Systemen und isothermen Vorgängen gilt unter Berücksichtigung von ![]() :
:
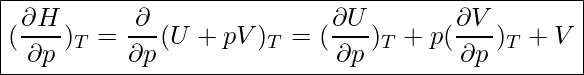
Inkompressibilität
Zur Erinnerung: Inkompressibilität bezeichnet die Eigenschaft eines Stoffes, unter Druckeinwirkung bei konstanter Temperatur sein Volumen nicht zu ändern, sich also nicht komprimieren zu lassen.
Das Volumen besteht hierbei aus immer derselben Anzahl von Teilchen (d. h. die Masse bleibt konstant).
Feststoffe und Flüssigkeiten
Feststoffe und Flüssigkeiten weisen beinahe immer die oben beschriebenen Eigenschaften auf, weshalb ![]() ausschließlich eine Funktion der Temperatur ist . Liegen Druckänderungen vor so gilt:
ausschließlich eine Funktion der Temperatur ist . Liegen Druckänderungen vor so gilt:
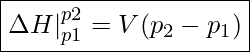
Gase
Die letzte Gleichung gilt nicht für Gase. Hier formulieren wir nachfolgende Gleichung:
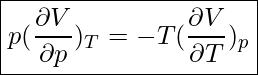
sowie
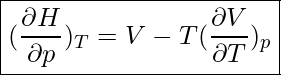
Ideales Gas
Im Falle eines idealen Gases gilt:
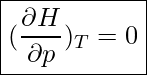
Die Technische Arbeit infolge adiabater Zustandsänderungen entspricht exakt der Enthalpieänderung.
![]()
Zudem entspricht der Wärmebetrag, sofern es sich um einen reinen Wärmeaustausch mit der Umgebung handelt, auch exakt der Enthalpieänderung.
![]()
Das heißt dann aber auch, finden Vorgänge zeitgleich statt, so gilt:
![]()
Nachdem wir dir jetzt alle Notwendige erklärt haben, schließen wir mit dieser Gleichung die Bilanzierung von Energieformen ab. Denn jetzt wenden wir uns im kommenden Kurstext der Exergiebilanz zu.
Was gibt es noch bei uns?
Was ist Technikermathe.de?
Unser Dozent Jan erklärt es dir in nur 2 Minuten!
Interaktive Übungsaufgaben
Quizfrage 1
Wusstest du, dass unter jedem Kursabschnitt eine Vielzahl von verschiedenen interaktiven Übungsaufgaben bereitsteht, mit denen du deinen aktuellen Wissensstand überprüfen kannst?
Auszüge aus unserem Kursangebot
Hat dir dieses Thema gefallen? – Ja? – Dann schaue dir auch gleich die anderen Themen zu den Kursen
ENT3 (Energetische Berechnungen) und
TM1 (Technische Mechanik – Statik) an.
Perfekte Prüfungsvorbereitung für nur 19,90 EUR/Jahr pro Onlinekurs
++ Günstiger geht’s nicht!! ++
Oder direkt >> Mitglied << werden und >> Zugriff auf alle 22 Kurse << (inkl. >> Webinare << + Unterlagen) sichern ab 8,90 EUR/Monat
++ Besser geht’s nicht!! ++
Technikermathe.de meets Social-Media
Dein Technikermathe.de-Team










